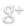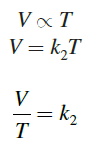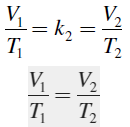Conociendo a Jacques Charles
Fue un químico, físico y matemático francés, nació el 12 de noviembre de 1746 en la ciudad de París. También fue un inventor ya que creo un aparato llamado densímetro que era capaz de medir la gravedad especifica de los fluidos líquidos. En el año 1783 rompió el récord del globo aerostático al elevarse a una altura de mas de 1.000 metros. Famoso por ser el descubridor previo de la famosa Ley de Charles, actualmente conocida como Ley de Charles y Gay-Lussac. Falleció en París el 7 de abril de 1823.

Animación: presión y masa constantes. Wikipedia.
Charles y Gay-Lussac
Los científicos Jacques Charles y Joseph Gay-Lussac estudiaron como se comportaba la presión y el volumen de un gas cuando variaba la temperatura.
Descubrieron que al calentar un gas el volumen de este se expandía, y al enfriarlo se contraía. Hablando cuantitativamente estos cambios resultaban muy coherentes.
Ellos notaron que a cualquier presión, la gráfica de volumen en función de la temperatura es una línea recta. Si llevamos la recta al volumen cero, siempre la intersección en el eje de la temperatura toma un valor de -273.15°C.
No importa la presión que utilizamos siempre tendremos una diferente recta pero una misma intersección en el eje de la temperatura.
Ley de Charles Gráfica
Tiempo después en el año 1848, Lord Kelvin comprendió este fenómeno. Nombro a la temperatura de -273,15°C como el Cero Absoluto que es la temperatura teóricamente mas baja posible.
Tomando al -237,15°C como punto de inicio, Lord Kelvin estableció una escala de temperatura. Denominada Escala Kelvin.
La Escala Kelvin es igual en magnitud a la Escala Celsius. Lo único que varia es el punto inicial de dicha escala.
| ESCALA | CELSIUS | KELVIN |
| CERO ABSOLUTO | -273,15°C | 0K (cero kelvin) |
| PUNTO CONGELACIÓN DEL AGUA | 0°C | 273,15K |
| PUNTO EBULLICIÓN DEL AGUA | 100°C | 373,15K |
Formula y Enunciado de la ley de Charles: Para Transformaciones Isobáricas (Presion Constante)
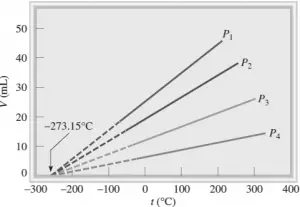
El volumen de un gas depende de la temperatura según la siguiente ecuación.
Esta ecuación enuncia que “El volumen de una cantidad fija de gas, a presión constante, es directamente proporcional a la temperatura absoluta del gas”
Dicha ecuación se la conoce como Ley de Charles y Gay Lussac, o simbólicamente, Ley de Charles. Donde K2 es la constante de proporcionalidad.
Para dos estados diferentes de un mismo gas, a una presión constante. Obtenemos esta formula que la que utilizaremos finalmente en todos los ejercicios de la ley de charles.
Formula y Enunciado de la ley de Charles: Para Transformaciones Isocóricas (Volumen Constante)
Otra forma de expresar la ley de Charles y Gay Lussac es de la siguiente manera.
Esta ley enuncia que: “La presión que ejerce un gas a volumen constante es directamente proporcional a la temperatura”.
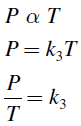 Para dos estados del gas obtenemos la siguiente expresión. Tambien utilizaremos esta formula para resolver los ejercicios de leyes de gases.
Para dos estados del gas obtenemos la siguiente expresión. Tambien utilizaremos esta formula para resolver los ejercicios de leyes de gases.
¿Para qué sirve la ley de charles?
Una breve explicación de la ley de Charles. Sirve para poder comprender como se comportan las moléculas del gas a someterse a altas presiones. Sabemos que las moléculas están separadas por grandes distancias (Ocupan mas volumen). Si aumentamos dicha presión las distancias entre las partículas es menor (Ocupan menos volumen).
Ejercicios y Problemas resueltos de la ley de Charles
LOS EJERCICIOS ESTARÁN DISPONIBLES EN UNOS DÍAS.